L-麦角硫因功效及多行业应用
发布时间:2023-11-13 点击数:1398
SeeBio公司L-麦角硫因(L-Ergothioneine,EGT, CAS: 497-30-3)是一种稀有的手性氨基酸,具有多重细胞生理保护功能,包括清除自由基、解毒、维护DNA的生物合成、促进细胞正常生长、增强细胞免疫系统、提供抗辐射、美白和抗衰老特性。由于其优良的性能,可以应用到许多领域。在化妆品领域可以用来抗衰老,可以作成防晒剂等产品。在医药领域可以用来处理炎症等,可以作成片剂、胶囊剂、口服制剂等;在保健品领域可以做成功能性食品,功能性饮品等产品,已被列入欧盟新资源食品清单。
EGT是一种稀有的天然手性氨基酸(含硫的组氨酸衍生物),化学结构式如下:
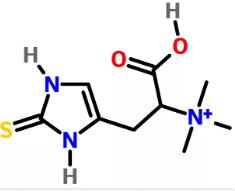
麦角硫因
EGT是一种在1909年发现的化合物,在真菌Claviceps purpurea中被检测到。纯品呈白色晶体,具有水溶性(在室温下可溶解0.9mol/L)。在生理pH值条件下和强碱性溶液中,EGT不会自我氧化。在其溶解状态下,存在硫酮和硫醇两种结构的互变异构。
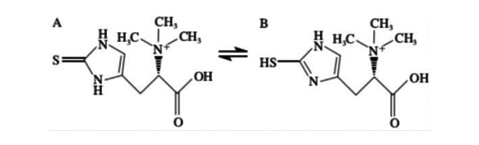
麦角硫因的硫酮和硫醇的互变异构体
麦角硫因的功效
高效的抗氧化剂:麦角硫因一直被认为是一种强大的低分子量抗氧化剂。它主要通过饮食摄入进入人体,能够在高水平氧化应激的细胞中积累。相对于其他抗氧化剂如白藜芦醇,麦角硫因具有更高的生物利用度。这是因为麦角硫因具有独特的生物特性,可以通过人体的皮肤细胞和组织中的OCTN1(麦角硫因转运体)来积累。与多数水溶性抗氧化剂不同,麦角硫因无法通过细胞膜渗透,而通过细胞中OCTN1转运。麦角硫因在人体内的抗氧化作用主要包括直接清除活性氧、螯合各种二价金属阳离子、激活抗氧化酶(如谷胱甘肽还原酶和线粒体超氧化物歧化酶)、以及抑制血红蛋白(如血红素和肌红蛋白)的氧化作用。
抑制紫外线引起的损伤以及细胞凋亡: 紫外线照射会激活多种生长因子和细胞因子受体相关的信号通路,引发DNA、蛋白质和脂质的损伤以及细胞凋亡。麦角硫因具有抑制由紫外线诱导的MMP-1(主要降解Ⅰ型胶原蛋白)和TNF-α(可促进炎症因子产生)等基因的表达能力,从而减少这些损伤的发生。它还具备抗光老化的能力,有效抑制紫外线照射引起的DNA、蛋白质和脂质损伤,以及细胞凋亡的过程。
对细胞的保护作用:麦角硫因还能 有效清除次氯酸,从而防止a 1-抗蛋白酶失活。研究显示,麦角硫因在体内一定浓度下发挥抗氧化作用,有效保护细胞免受氧化损伤。对抗次氯酸的清除能力使其成为强大的保护剂,特别是对于a 1-抗蛋白酶这类对次氯酸敏感的酶,麦角硫因能有效保护其免受次氯酸引发的失活作用。由于中性粒细胞是体内次氯酸的主要来源,麦角硫因的作用之一是保护红细胞不收到来自正常功能或病态炎症部位的中性粒细胞的危害。
详询西宝产品,请咨询:400-021-8158 / 021-50272975。
品名 | CAS号 | 级别 | 包装 |
L-麦角硫因 L-Ergothioneine | 497-30-3 | 化妆品级,98% | 100g, 500g, 1kg, 5kg |
食品级,98% |
通过清除活性氧族、螯合金属离子、激活抗氧化物酶、抑制超氧化物歧化酶以及抑制血红素蛋白的氧化反应,麦角硫因表现出强大的抗氧化活性。这些特性使其在化妆品、生物医药、食品饮料、功能食品及生物技术等领域具有广泛的用途和市场前景。
化妆品行业应用
麦角硫因(EGT)在化妆品中被广泛应用作抗氧化剂,特别用于护肤产品。它通过清除自由基,有效减轻氧化应激,降低紫外线引起的皮肤损伤和老化迹象。EGT还提高皮肤细胞的抵抗力,减少DNA、蛋白质和脂质损伤,有助于DNA修复,提高细胞的存活率,促进皮肤健康。作为一种天然的抗氧化成分,EGT在化妆品中的应用有助于保护皮肤免受环境应激因素的侵害,维持皮肤的年轻和健康。
保护皮肤:L-麦角硫因(EGT)在化妆品中被广泛应用作抗氧化剂,特别用于护肤产品。它通过清除自由基,有效减轻氧化应激,降低紫外线引起的皮肤损伤和老化迹象。EGT还提高皮肤细胞的抵抗力,减少DNA、蛋白质和脂质损伤,有助于DNA修复,提高细胞的存活率,促进皮肤健康。作为一种天然的抗氧化成分,EGT在化妆品中的应用有助于保护皮肤免受环境应激因素的侵害,维持皮肤的年轻和健康。
避免紫外线诱导的ROS损害:L-麦角硫因(稳定存在于食品植物和那些受到相对高水平氧化应激的动物组织中。与伊地那韦作为抗氧化剂辅酶Q10的类似物相比,它们都被广泛应用于护肤产品,但它们的相对效力一直缺乏详细描述。研究表明,在培养的人类成纤维细胞中,存在OCTN-1,这是EGT的特定受体/转运蛋白,易于检测。EGT在抑制脂质过氧化的形成方面表现更为高效,与伊地那韦相比,EGT处理后的样品在加入抗氧化剂H2O2后的120分钟内显然产生较少的过氧化物。此外,EGT在经受UVA340辐照后更快速、更有效地捕获活性氧自由基(ROS)。因此,由于OCTN-1在成纤维细胞中存在,EGT被认为是一种天然皮肤抗氧化剂。相对于辅酶Q10和伊地那韦,EGT以更高效的方式直接清除自由基,从而保护细胞免受紫外线诱导的ROS的损害。
延缓皮肤衰老:L-麦角硫因(EGT)是一种含硫氨基酸,被视为自然界的抗氧化剂。这种独特的氨基酸具有清除自由基的能力,同时还能够保护细胞免受紫外线辐射引发的氧化应激。在相关研究中,EGT被发现可以清除超氧自由基(•O2–)和单线态氧(1O2)。在细胞培养中,EGT成功地抑制了UVB辐照引起的肿瘤坏死因子-α(TNF-α)的上调。此外,EGT还在暴露于UV-A的纤维细胞中成功抑制了近50%的基质金属蛋白酶-1(MMP-1)蛋白表达,并减少了MMP-1 mRNA的表达水平。这一研究表明,EGT能够清除由I型和II型光敏化产生的活性氧种,同时抑制TNF-α和MMP-1的表达,从而减少紫外线辐射引发的皮肤衰老效应。
皮肤护理和抗光老化成分:与细胞水平的衰老相关的变化往往与线粒体的生理状态密切相关。在这些变化中,一种常见的线粒体DNA损伤类型是所谓的“常见缺失”,指的是线粒体DNA中4977个碱基对的缺失。在皮肤细胞中,这种现象通常是由紫外线引起的线粒体DNA氧化损伤所致。研究的目标是评估抗氧化剂L-麦角硫因对紫外线引发的皮肤细胞损伤的影响。研究还关注了L-麦角硫因对还原型谷胱甘肽水平的影响,并通过聚合酶链反应的方式检测了人类成纤维细胞中是否存在“常见缺失”。结果显示,L-麦角硫因提高了细胞内还原型谷胱甘肽水平,并有效地保护细胞免受与光老化相关的线粒体DNA“常见缺失”的诱发。综合研究结果,L-麦角硫因可能成为一种有效的皮肤护理和抗光老化成分。
保护表皮角质细胞:L-麦角硫因一直被认为是一种强大且稳定的低分子量抗氧化剂。人体通过饮食摄入L-麦角硫因,并它会在通常受到高水平氧化应激的细胞中积累。然而,由于L-麦角硫因无法穿透细胞膜,它的保护功能受限于只有表达L-麦角硫因专门受体/转运蛋白OCTN1的细胞。研究观察到,皮肤细胞中的表皮角质细胞也具备合成OCTN1的能力,这使它们能够内化和积累L-麦角硫因。这种积累赋予细胞更强的抗氧化能力,降低了表皮角质细胞在受到模拟太阳紫外线氧化应激时的活性氧种、DNA、蛋白质和脂质损伤水平。L-麦角硫因不仅可以预防氧化损伤,还可能促进紫外线照射下的细胞DNA修复。这减少了细胞成分的氧化损伤,限制了细胞凋亡反应,提高了细胞的存活率。细胞具备吸收、积累和利用强大抗氧化剂L-麦角硫因的能力,使这种天然氨基酸及其受体/转运蛋白成为皮肤抗氧化防御系统的重要组成部分。
生物医药行业应用
L-麦角硫因(EGT)在生物制药领域有广泛应用。EGT显示出潜在的抗氧化和抗炎正面影响,特别在2型糖尿病及其并发症的处理中。研究发现EGT单独或与降糖药联合使用可降低肾脏和肝脏损伤,改善血糖控制,减少氧化应激和炎症反应,有望减轻2型糖尿病相关并发症。后续仍需要进一步研究以解决EGT的处理剂量、OCTN1受体的调控机制以及其在肠道微生物中的影响等相关问题。
潜在的抗氧化和抗炎正面影响:L-麦角硫因(EGT)在生物制药领域有广泛应用。EGT显示出潜在的抗氧化和抗炎正面影响,特别在2型糖尿病及其并发症的处理中。研究发现EGT单独或与降糖药联合使用可降低肾脏和肝脏损伤,改善血糖控制,减少氧化应激和炎症反应,有望减轻2型糖尿病相关并发症。后续仍需要进一步研究以解决EGT的处理剂量、OCTN1受体的调控机制以及其在肠道微生物中的影响等相关问题。
减轻肾脏功能损害:L-麦角硫因 (L-EGT) 是一种食品和药物管理局批准的补充剂,具有细胞保护、抗氧化和抗炎特性。 研究调查了其在 2 型糖尿病 (T2D) 大鼠模型中的肾损伤保护作用,研究 L-egt 单独使用或与降糖药联合使用对 2 型糖尿病 (T2D) 大鼠模型肾损伤的保护作用。 使用果糖-链脲佐菌素大鼠模型在雄性 Sprague-Dawley 大鼠中诱导 T2D。 L-egt 单独或与降糖药联合给药。实验结果表明,L-egt单独或与降糖药联合使用可减轻肾脏功能损害,降低高血糖,改善处理效果,同时提高抗氧化和抗炎基因的表达。因此,L-egt与降糖药的联合使用可能作为减轻2型糖尿病肾损伤的辅助疗法。
处理肝脏并发症:研究评估了L-麦角硫因 (L-egt) 以及其与降糖药联合使用对2型糖尿病(T2D)大鼠的肝脏保护作用。结果显示,L-egt单独或与降糖药联合使用可以减少肝脏肥大、肝损伤、甘油三酯水平、氧化应激和炎症。此外,对糖尿病大鼠联合给予 L-egt 和降糖药可降低血糖和胰岛素抵抗。 这些研究结果支持了L-egt在处理与T2D相关的肝脏并发症中的潜在作用。
应对紫外线诱导的细胞反应:麦角硫氨酸 (EGT) 是一种含硫氨基酸,被认为具有天然抗氧化剂的作用。 本研究的目的是确定抗氧化活性的性质并研究 EGT 对紫外线诱导的细胞反应的影响。 在化学研究中,EGT 清除超氧阴离子自由基(中心点 O-2(-))和单线态氧(O-1(2))。 在培养的成纤维细胞中,EGT 通过 UVB 照射抑制 TNF-α 的上调。 此外,在暴露于 UV-A 的成纤维细胞中,EGT 将基质金属蛋白酶 I (MMP-1) 蛋白的表达抑制近 50%,并减少 MMP-1 mRNA 的表达。 从这些结果中,我们得出结论,EGT 清除 I 型和 11 型光敏化产生的活性氧,并在转录水平抑制 TNF-α 表达和 MMP-1。 EGT 可能通过清除中心点 O-2(-) 和 O-1(2) 来降低紫外线照射后皮肤的抗衰老作用,并减少蛋白酶和炎症活性的信号。
预防氧化应激相关疾病:EGT作为一种天然抗氧化剂,在处理或预防氧化应激相关疾病方面表现出良好的潜力,其抗氧化功能明显优于其他天然抗氧化剂。尽管已经在医药和化妆品行业广泛使用,但在应对一系列未解决问题时,EGT的应用还存在挑战。这些问题包括研究蘑菇中其他可能有益的成分、明确EGT的处理剂量与疾病之间的关系、探索OCTN1表达的调控机制以及揭示EGT可能存在的其他作用机制。此外,对EGT对肠道微生物的影响也需要更多研究。
食品行业应用
L-麦角硫因已在欧洲获得新型食品认可,证明其在食品领域的安全性。相关研究估算了各年龄组从新型食品中摄入L-麦角硫因的每日量,发现均低于安全水平(NOAEL)。此外,研究还强调L-麦角硫因对糖尿病孕鼠的胚胎发育异常有预防作用,同时支持其作为牛奶热处理的指标。这一系列研究结果坚定了L-麦角硫因在食品领域作为安全有效成分的地位。
L-麦角硫因已在欧洲获得新型食品认可,证明其在食品领域的安全性。相关研究估算了各年龄组从新型食品中摄入L-麦角硫因的每日量,发现均低于安全水平(NOAEL)。此外,研究还强调L-麦角硫因对糖尿病孕鼠的胚胎发育异常有预防作用,同时支持其作为牛奶热处理的指标。这一系列研究结果坚定了L-麦角硫因在食品领域作为安全有效成分的地位。
根据欧洲委员会的要求,饮食产品、营养和过敏委员会(NDA)对合成L-麦角硫因作为新型食品的补充膳食摄入和安全性进行评估。研究估算了这些人群从新型食品中摄入的L-麦角硫因的顶值每日摄入量,另加上背景膳食。结果显示,婴儿每天摄入2.82 mg/kg体重、幼儿为3.39 mg/kg体重、成年人(包括孕妇和哺乳妇女)为1.31 mg/kg体重。基于多方位的毒理数据,委员会认为原评估中确定的每天800 mg/kg体重的无观察到不良作用水平(NOAEL)同样适用于孕妇、哺乳妇女、幼儿和婴儿。相应的暴露边际足够大,分别为婴儿284、幼儿236和孕妇以及哺乳妇女610。因此,委员会得出结论,合成L-麦角硫因新型食品在婴儿、幼儿、孕妇和哺乳妇女的拟议使用和摄入水平下是安全的。
此外,NDA就合成L-麦角硫因(Ergoneine (R))提供了一份科学意见,将其作为新型食品提交。这种新型食品的合成L-麦角硫因通过一种一锅法专利制造工艺生产,它是硫醇组氨酸的衍生物,天然存在于多种食物中,如蘑菇、一些豆类、杂碎和谷物。新型食品的生产过程和成分等方面满足要求,不引起安全担忧。申请人打算在饮料、谷物棒、牛奶、乳制品和巧克力中每份食品中使用高达5毫克的新型食品。此外,他们还提议将其作为食品补充剂提供给3岁以上的儿童和普通成人,不包括孕妇和哺乳妇女。基于大鼠的亚慢性毒性研究,结合来自所有来源的L-麦角硫因的摄入水平,委员会得出结论,该新型食品在拟议使用条件下是安全的,成年人(不包括孕妇和哺乳妇女)的安全边际为470,3岁以上的儿童为216。
生殖安全研究:L-麦角硫因是由细菌和真菌合成,并存在于许多人类食物中。我们通过饮食途径在大鼠中评估了自然同源L-麦角硫因的生殖安全性。在怀孕的前10周内,每天以1.147毫克/kg体重的L-麦角硫因给予糖尿病孕鼠,结果降低了胚胎畸形的发生率,使其达到与非糖尿病动物相近的水平。L-麦角硫因对血浆葡萄糖水平没有影响,不论是对于糖尿病动物还是对照组的动物都没有影响。我们得出结论,L-麦角硫因通过抑制葡萄糖介导的自由基依赖的胚胎畸形,起到了重要的抗氧化预防作用机制,结合维生素E的使用可能有助于管理糖尿病胚胎病变。
对胚胎发育的影响:自然抗氧化剂麦角硫因对糖尿病孕鼠的胚胎发育异常的影响。通过将糖尿病孕鼠每天补充1.147毫克/kg体重的L-麦角硫因,仅在妊娠的前11.5天内,成功降低了胚胎畸形的发生率,使其达到与非糖尿病动物相近的水平。麦角硫因没有对糖尿病和对照动物的血浆葡萄糖水平产生影响。而研究结论则是,麦角硫因通过抑制葡萄糖介导的自由基依赖性胚胎畸形,发挥了重要的抗氧化防治作用,结合维生素E的使用可能有助于管理糖尿病引起的胚胎病变。
牛奶热处理的指标:创建了一种高效而敏感的毛细管超性能液相色谱(HILIC-UPLC)方法,用于在商业牛奶中测定L-麦角硫因(ERT)。在对ERT进行衍生后,采用100x2.1毫米Waters Cortecs UPLC HILIC 1.6微米柱,使用30 mmol/L乙酸铵/乙腈(10:90,体积比)的混合物作为等温流动移动相,成功实现了不到5分钟的色谱分离。该方法的检测限和定量限分别为0.03和0.10微摩尔/升。在0.16至5.08微摩尔/升的浓度范围内,该方法呈线性关系。我们在不同类别的商业牛奶中平均检测到ERT的浓度为0.442±0.191微摩尔/升,其中超高温牛奶含量较高,而未经处理和HTST全脂牛奶中含量较低。研究表明ERT可作为牛奶热处理的指标。
L-(+) 麦角硫因是一种天然存在的硫醇氨基酸,具有抗氧化特性和作为膳食补充剂的潜在益处。 的研究调查了它的毒理学和致突变潜力。结果表明,L-(+) 麦角硫因及其天然仿生剂经过多项实验,包括细菌突变试验和动物实验,均未显示出毒性或致突变性。因此,这种物质在建议的剂量下在动物体内具有良好的耐受性,支持其作为潜在安全的膳食补充剂。
其他应用:
用于器官移植方面:现有的组织的保存量和保存时间对于器官移植手术的成功起到了决定性的作用。保存器官移植方面用的较多的抗氧化剂是谷胱甘肽,当它暴露于环境中是,极易被氧化,即使在冷藏或者是液体环境下,其抗氧化能力也是大大下降,对细胞产生毒性并且产生炎症,诱导组织蛋白的水解。而麦角硫因恰似一种在水溶液中稳定,还可以螯合重金属离子的抗氧化剂,在器官保护领域可以作为谷胱甘肽的替代品,更好的实现移植器官的保护。
在眼科方面的应用: 几年研究发现,麦角硫因在对眼睛的保护方面起到了关键性的作用,因此很多研究者希望能够开发出一种眼科产品,以促进眼科处理手术的发展。眼科手术一般是局部进行,而麦角硫因的水溶性和稳定性为进行这种手术提供了可行性,具有很大的应用价值。
参考文献:
[1]. K. Bazela, et al. L-Ergothioneine Protects Skin Cells against UV-Induced Damage—A Preliminary Study. DOI:10.3390/COSMETICS1010051
[2]. Kei Obayashi, et al. L-Ergothioneine scavenges superoxide and singlet oxygen and suppresses TNF-alpha and MMP-1 expression in UV-irradiated human dermal fibroblasts. DOI:10.1111/J.0142-5463.2005.00265_2.X
[3]. K. Dong, et al. A comparison of the relative antioxidant potency of L-ergothioneine and idebenone. DOI:10.1111/j.1473-2165.2007.00330.x
[4]. N. Markova, et al. Skin cells and tissue are capable of using L-ergothioneine as an integral component of their antioxidant defense system. DOI:10.1016/j.freeradbiomed.2009.01.021
[5]. A. Dare, et al. L-ergothioneine and its combination with metformin attenuates renal dysfunction in type-2 diabetic rat model by activating Nrf2 antioxidant pathway. DOI:10.1016/j.biopha.2021.111921
[6]. A. Dare, et al. L-ergothioneine and metformin alleviates liver injury in experimental type-2 diabetic rats via reduction of oxidative stress, inflammation, and hypertriglyceridemia. DOI:10.21203/RS.3.RS-480961/V1
[7]. Kei Obayashi, et al. L-Ergothioneine scavenges superoxide and singlet oxygen and suppresses TNF-alpha and MMP-1 expression in UV-irradiated human dermal fibroblasts. DOI:10.1111/J.0142-5463.2005.00265_2.X
[8]. Tong-Tong Fu, et al. Ergothioneine as a Natural Antioxidant Against Oxidative Stress-Related Diseases. DOI:10.3389/fphar.2022.850813
[9]. D. Turck, et al. Safety of synthetic l-ergothioneine (Ergoneine®) as a novel food pursuant to Regulation (EC) No 258/97. DOI:10.2903/J.EFSA.2016.4629
[10]. D. Turck, et al. Statement on the safety of synthetic l-ergothioneine as a novel food – supplementary dietary exposure and safety assessment for infants and young children, pregnant and breastfeeding women. DOI:10.2903/j.efsa.2017.5060
[11]. R. Forster, et al. Reproductive safety evaluation of L-Ergothioneine. DOI:10.1016/j.fct.2015.02.019
[12]. M. Guijarro, et al. Effects of ergothioneine on diabetic embryopathy in pregnant rats. DOI:10.1016/S0278-6915(02)00177-1
[13]. S. Sotgia, et al. Ultra-performance liquid chromatographic determination of L-ergothioneine in commercially available classes of cow milk. DOI:10.1111/1750-3841.12564
[14]. P. Marone, et al. A Safety Evaluation of a Nature-Identical l-Ergothioneine in Sprague Dawley Rats. DOI:10.1177/1091581816653375
[2]. Kei Obayashi, et al. L-Ergothioneine scavenges superoxide and singlet oxygen and suppresses TNF-alpha and MMP-1 expression in UV-irradiated human dermal fibroblasts. DOI:10.1111/J.0142-5463.2005.00265_2.X
[3]. K. Dong, et al. A comparison of the relative antioxidant potency of L-ergothioneine and idebenone. DOI:10.1111/j.1473-2165.2007.00330.x
[4]. N. Markova, et al. Skin cells and tissue are capable of using L-ergothioneine as an integral component of their antioxidant defense system. DOI:10.1016/j.freeradbiomed.2009.01.021
[5]. A. Dare, et al. L-ergothioneine and its combination with metformin attenuates renal dysfunction in type-2 diabetic rat model by activating Nrf2 antioxidant pathway. DOI:10.1016/j.biopha.2021.111921
[6]. A. Dare, et al. L-ergothioneine and metformin alleviates liver injury in experimental type-2 diabetic rats via reduction of oxidative stress, inflammation, and hypertriglyceridemia. DOI:10.21203/RS.3.RS-480961/V1
[7]. Kei Obayashi, et al. L-Ergothioneine scavenges superoxide and singlet oxygen and suppresses TNF-alpha and MMP-1 expression in UV-irradiated human dermal fibroblasts. DOI:10.1111/J.0142-5463.2005.00265_2.X
[8]. Tong-Tong Fu, et al. Ergothioneine as a Natural Antioxidant Against Oxidative Stress-Related Diseases. DOI:10.3389/fphar.2022.850813
[9]. D. Turck, et al. Safety of synthetic l-ergothioneine (Ergoneine®) as a novel food pursuant to Regulation (EC) No 258/97. DOI:10.2903/J.EFSA.2016.4629
[10]. D. Turck, et al. Statement on the safety of synthetic l-ergothioneine as a novel food – supplementary dietary exposure and safety assessment for infants and young children, pregnant and breastfeeding women. DOI:10.2903/j.efsa.2017.5060
[11]. R. Forster, et al. Reproductive safety evaluation of L-Ergothioneine. DOI:10.1016/j.fct.2015.02.019
[12]. M. Guijarro, et al. Effects of ergothioneine on diabetic embryopathy in pregnant rats. DOI:10.1016/S0278-6915(02)00177-1
[13]. S. Sotgia, et al. Ultra-performance liquid chromatographic determination of L-ergothioneine in commercially available classes of cow milk. DOI:10.1111/1750-3841.12564
[14]. P. Marone, et al. A Safety Evaluation of a Nature-Identical l-Ergothioneine in Sprague Dawley Rats. DOI:10.1177/1091581816653375
上一篇:MSC相关小分子化合物
下一篇:CiMS(TM) 人间充质干细胞用无血清培养基